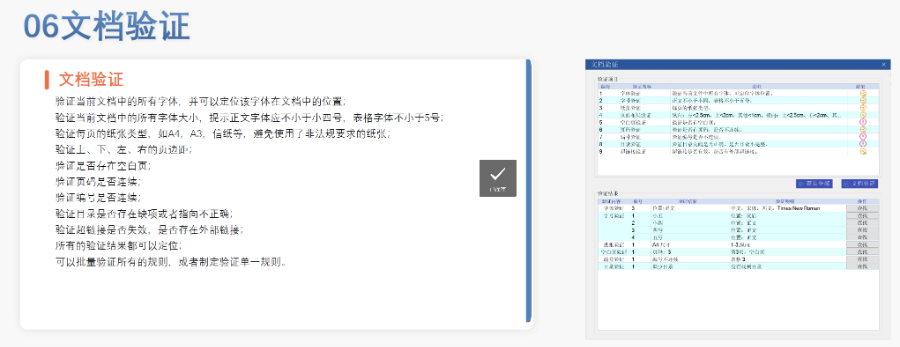
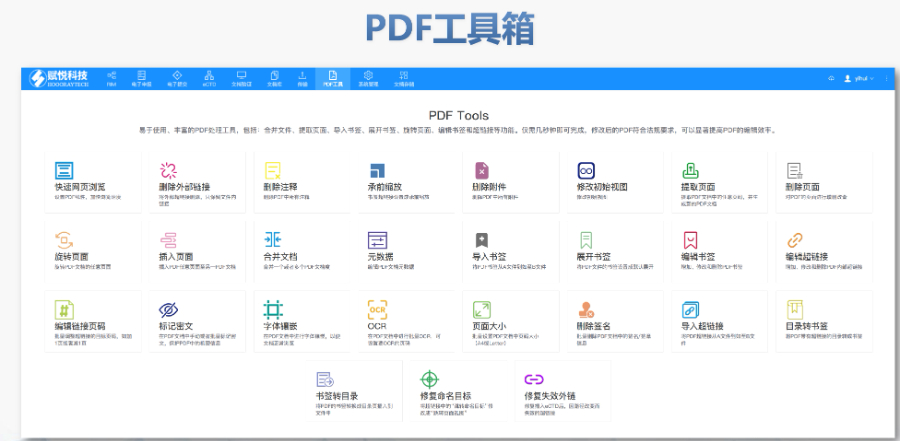
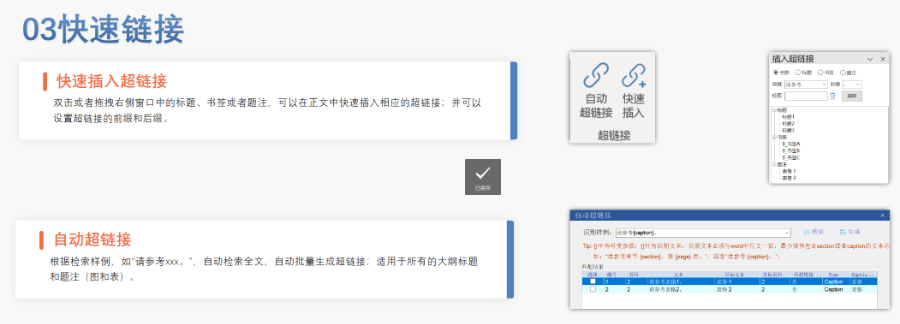
PDF工具箱 批量處理與格式修復 支持PDF合并、拆分、提取頁面、旋轉頁面等操作,可批量修復字體未嵌入、超鏈接錯誤等問題,確保文件符合藥品注冊法規(guī)要求。 智能書簽與超鏈接管理 提供書簽導入/導出、超鏈接自動生成(支持關鍵字搜索定位鏈接)、題注超鏈接拖拽式編輯等功能,簡化復雜文檔的導航設計。 文檔轉換與OCR識別 支持Word轉PDF(自動生成書簽、嵌入字體),以及PDF與Word、Excel等格式互轉,集成OCR功能用于掃描件文字識別。 合規(guī)性驗證 自動驗證PDF的頁面布局、頁碼連續(xù)性、空白頁、目錄層級等屬性,并定位具體錯誤位置,減少人工檢查成本。 安全與協(xié)作功能 支持文檔加密、數(shù)字簽名、云端同步及多設備共享,滿足企業(yè)級文件安全管理需求。澳大利亞的eCTD申報相關技術支持。黑龍江國產eCTD
審評效率與時間線優(yōu)化 eCTD的標準化縮短了審評周期:集中程序平均審評時間從18個月降至12個月,互認程序可在90天內完成成員國意見協(xié)調。自動化驗證工具減少了格式錯誤導致的退審率,但復雜藥學數(shù)據(jù)的科學審評仍需較長時間。申請人可通過預提交會議(Pre-submission meeting)提前溝通技術細節(jié),規(guī)避潛在延誤。 區(qū)域協(xié)作與全球互認 歐盟通過互認程序與澳大利亞、加拿大等國實現(xiàn)eCTD數(shù)據(jù)共享,CEP證書在40余個非歐盟國家有效。然而,模塊一區(qū)域信息的差異性仍要求申請人定制化調整,例如亞洲國家可能要求附加穩(wěn)定性研究數(shù)據(jù)。ICH的協(xié)調作用有助于減少重復提交,但完全全球化仍需解決法規(guī)和技術壁壘。 技術工具與行業(yè)生態(tài) 主流eCTD編輯軟件(如Lorenz、Extedo)支持歐盟區(qū)域模板的自動化生成,并與驗證工具集成實現(xiàn)一鍵校驗。云平臺解決方案逐漸普及,支持多國團隊協(xié)同編輯和實時版本控制。然而,軟件采購和維護成本較高,中小企業(yè)常選擇外包給專業(yè)服務商完成遞交。浙江藥品注冊eCTD供應商瑞士NDA注冊申報相關技術支持。
eCTD的技術架構與模塊要求:美國eCTD基于XML技術,嚴格遵循ICH M4框架,分為5個模塊:模塊1(地區(qū)行政信息)、模塊2(技術總結)、模塊3-5(質量、非臨床與臨床數(shù)據(jù))。其中,模塊1需包含F(xiàn)DA特定的us-regional.xml文件,涵蓋申請編號、聯(lián)系人和DMF授權書等行政信息。模塊2-5需與ICH CTD全球統(tǒng)一標準一致,但FDA對文件顆粒度要求更細,例如非臨床研究報告需拆分并標記Study ID。PDF文件需符合FDA v4.1格式規(guī)范,包括字體嵌入、書簽層級和超鏈接功能。
技術壁壘與興市場挑戰(zhàn) 非洲和東南亞國家逐步采納eCTD,但其IT基礎設施薄弱導致實施進度滯后。歐盟通過“eCTD全球化倡議”提供技術援助,幫助興市場建立驗證體系和培訓中心。跨國藥企需針對不同區(qū)域定制遞交策略,例如在模塊1附加本地穩(wěn)定性數(shù)據(jù)。 監(jiān)管科學與創(chuàng)激勵 eCTD支持真實世界證據(jù)(RWE)和適應性臨床試驗設計的整合,加速創(chuàng)藥上市。EMA的PRIME計劃為突破性療法提供eCTD快速通道,允許分階段提交模塊數(shù)據(jù)。孤兒藥和兒科藥的eCTD序列可享受費用減免和優(yōu)先審評。 供應鏈安全與審計追蹤 eCTD的XML主干文件記錄所有提交版本,支持供應鏈問題的追溯分析。原料藥CEP持有者需及時更變更信息,確保下游制劑廠商獲取數(shù)據(jù)。區(qū)塊鏈技術試點用于追蹤eCTD數(shù)據(jù)流,防止篡改和未授權訪問。 文化差異與實施障礙 部分南歐國家偏好傳統(tǒng)紙質流程,導致eCTD推廣阻力較大。EMA通過多語種培訓材料和區(qū)域協(xié)調員制度促進文化適應。行業(yè)需調整管理思維,將eCTD從“合規(guī)負擔”轉化為“競爭優(yōu)勢”。加拿大eCTD申報相關技術支持。
DMF維護與合規(guī) 年度更 即使無變更,每年需提交聲明;重大工藝/設施變更需及時通知客戶并更文件。 現(xiàn)場檢查 原料藥企業(yè)需通過FDA現(xiàn)場檢查,驗證是否符合ICH Q7 GMP標準,并與DMF內容一致。 轉讓與關閉 轉讓:需書面通知FDA并提供持有者信息。 關閉:未提交年度報告或持有人主動申請,需說明原因并通知所有授權方。 關鍵注意事項 數(shù)據(jù)質量:所有資料需準確、完整,減少審核延遲風險。 合規(guī)性:遵循FDA指南(如21 CFR Part 207)及USP標準(如培養(yǎng)基物料來源級別)。 溝通機制:建議通過專業(yè)機構(如瑞歐佰藥)協(xié)助,定期提交周報并制定計劃表以提高效率。 常見問題解答 生物制品分類:培養(yǎng)基、外泌體等均屬Ⅱ類DMF。 質量標準:參考USP及同行標準,需提供分析方法驗證及雜質對比研究。 周期估算:資料準備約5-50個工作日,總周期受缺陷回復影響。歐盟NDA注冊申報相關技術支持。上海藥品注冊eCTD銷售電話
歐盟eCTD注冊咨詢相關技術支持。黑龍江國產eCTD
經濟影響與成本效益 盡管初期投入較高(平均每企業(yè)需50萬歐元),但eCTD可減少30%的審評延遲成本,長期效益。仿制藥企業(yè)通過eCTD復用原研數(shù)據(jù),節(jié)省80%的申報準備時間。歐盟預算撥款2億歐元資助中小企業(yè)完成數(shù)字化轉型。 倫理審查與數(shù)據(jù)隱私 eCTD中的患者數(shù)據(jù)需匿名化處理,符合《通用數(shù)據(jù)保護條例》(GDPR)要求。臨床試驗模塊(模塊5)的提交需附帶倫理委員會批準文件,且區(qū)域版本需體現(xiàn)各國倫理審查差異。AI輔助匿名化工具在保護隱私的同時提升數(shù)據(jù)處理效率。 技術融合與跨領域應用 eCTD格式擴展至醫(yī)療器械和保健品領域,歐盟試點eCTD-MDR項目整合ISO標準。基因產品的eCTD需附加生物安全數(shù)據(jù)庫,并與歐盟基因庫實時同步。未來,eCTD或與電子健康檔案(EHR)系統(tǒng)對接,支持個性化用藥。 持續(xù)改進與行業(yè)反饋機制 EMA每年發(fā)布eCTD實施報告,分析常見錯誤并更指南。行業(yè)聯(lián)盟(如EFPIA)通過定期研討會向監(jiān)管機構反饋技術痛點,推動標準優(yōu)化。開放式API接口的推廣將促進eCTD工具鏈的互操作性,降低技術鎖定風險。黑龍江國產eCTD