常用蛋白表達陽性
無細胞蛋白表達技術(CFPS)在毒性蛋白和膜蛋白的合成中展現出獨特優勢。傳統細胞系統難以表達具有細胞毒性的蛋白(如溶菌酶、限制性內切酶),而無細胞蛋白表達技術通過體外開放環境規避了宿主細胞存活限制,可高效合成活性毒蛋白,例如珀羅汀生物成功表達的BamHI內切酶,其Minimun活性濃度只需0.001μg/μL。此外,無細胞蛋白表達技術通過添加表面活性劑或脂質體模擬膜環境,實現了全長跨膜蛋白(如CLDN18.1)的可溶表達,純度達80%以上,為藥物靶點開發提供了關鍵工具。優化后的??原核體外蛋白表達??已廣泛應用于抗體篩選、酶工程等領域。常用蛋白表達陽性
國內生物醫藥行業對CFPS的價值認知不足,傳統企業更依賴成熟的細胞表達系統(如CHO、大腸桿菌)。許多藥企認為無細胞蛋白表達技術只適用于“科研級小試”,對其在藥物開發(如ADC定點偶聯)、mRNA疫苗抗原快速制備等工業化潛力持觀望態度。同時,無細胞蛋白表達技術在復雜蛋白表達(如糖基化抗體)上的局限性也削弱了市場信心。相比之下,歐美已形成“CRO+藥企”的協同生態(如Moderna與CFPS服務商合作),而國內缺乏此類模范案例,導致技術推廣缺乏驅動力。內源蛋白表達產業鏈大腸桿菌裂解物是??同位素標記蛋白表達??的首要方案,因快速反應能zai大化標記原子利用率。

無細胞蛋白表達技術(CFPS)的操作確實比傳統細胞表達更繁瑣,主要體現在多步驟的體系配置上。實驗者需要精確配制包含裂解物、能量混合物(ATP/GTP)、氨基酸、輔因子(Mg2?、K?)和DNA/mRNA模板的復雜反應體系,且各組分濃度需嚴格優化(如Mg2?濃度波動1 mM就可能導致表達失敗)。此外,裂解物制備本身涉及細胞培養、破碎、離心透析等步驟,若直接購買商業化裂解物(如RTS 100),單次成本可能高達數百元。對于新手而言,反應條件的微調(pH、溫度、氧化還原環境)往往需要多次試錯,增加了實驗難度。
盡管前景廣闊,無細胞蛋白表達技術市場仍面臨成本控制和規模化生產的挑戰。目前反應體系依賴昂貴的裂解物和能量試劑,限制了大規模應用,但新型工程化裂解物(如敲除核酸酶的E. coli提取物)和能量再生系統的開發有望降低成本。未來,無細胞蛋白表達技術技術可能與AI驅動的蛋白設計、連續生物制造工藝結合,進一步拓展在細胞zhi liao、人造肉(如無細胞合成血紅蛋白)等新興領域的應用。Goverment與資本對生物制造的投入(如美國《國家生物技術和生物制造計劃》)也將加速無細胞蛋白表達技術的商業化進程,使其成為千億美元合成生物學市場的重要支柱技術。芯片級體外蛋白表達??體現較前沿的進展。

無細胞蛋白表達技術的模板可以是線性DNA(如PCR產物)或環狀質粒,需包含啟動子(如T7/T3/SP6)和核糖體結合位點(RBS)以啟動轉錄翻譯。為提升效率,系統可能添加分子伴侶(如DnaK/GroEL)輔助蛋白折疊,或氧化還原劑(如谷胱甘肽)促進二硫鍵形成。部分高級系統(如PURE體系)使用純化重組元件替代粗提物,實現更高可控性,但成本較高。無細胞蛋白表達技術可靈活引入非天然氨基酸(nnAA),擴展了蛋白質的功能多樣性。例如,通過定制tRNA和氨酰-tRNA合成酶,無細胞蛋白表達技術系統能準確將熒光標記或交聯基團嵌入目標蛋白,用于結構生物學或藥物偶聯開發。更前沿的應用是人工生命體系的構建,如利用無細胞蛋白表達技術合成噬菌體或人工細胞雛形,結合微流控技術模擬細胞內代謝網絡,為合成生物學研究提供可控的簡化模型。體外蛋白表達技術正在改寫蛋白質研究的??時空規則??。無細胞蛋白表達的優勢
對于需糖基化的抗體,??哺乳細胞體外表達??比原核系統更適用。常用蛋白表達陽性
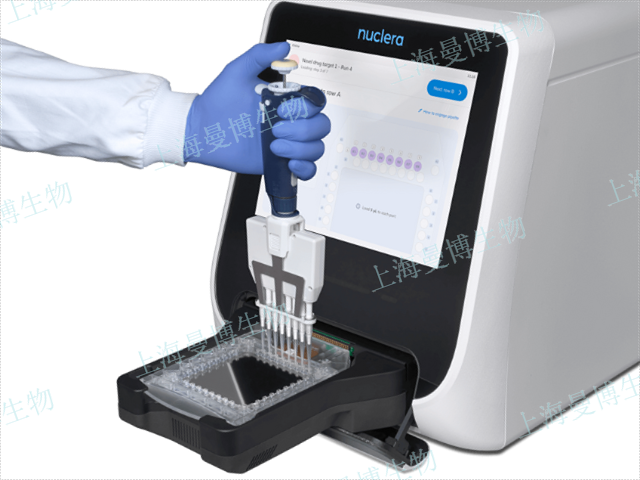
從裂解物來源看,無細胞蛋白表達技術主要分為原核系統和真核系統。原核系統以大腸桿菌S30提取物為主,成本低、耐受性強,適合表達簡單蛋白或引入非天然氨基酸,但缺乏復雜翻譯后修飾能力。真核系統包括兔網織紅細胞裂解物(RRL)和麥胚提取物(WGE),前者適合哺乳動物蛋白的高效表達,后者對植物和病毒蛋白更優,且能處理長鏈RNA,但成本較高。此外,昆蟲細胞提取物系統近年也用于復雜蛋白的修飾研究。英國nuclera 高通量微流控蛋白表達篩選系統可助力支持無細胞蛋白表達技術,如想了解更多信息,歡迎咨詢官方代理商上海曼博生物!常用蛋白表達陽性
- 大腸桿菌可溶蛋白表達發展前景 2025-07-12
- 293蛋白表達上調 2025-07-12
- gst融合蛋白表達實驗流程 2025-07-12
- 低溫誘導蛋白表達陰性 2025-07-12
- 大腸桿菌可溶蛋白表達修飾 2025-07-12
- 酵母蛋白表達陽性 2025-07-12
- 大腸桿菌蛋白表達修飾 2025-07-12
- 差異蛋白表達上調 2025-07-12
- 高通量蛋白表達修飾 2025-07-12
- 融合蛋白表達包涵體 2025-07-12
- 天津鼻噴制劑輔料生產廠家 2025-07-12
- 武漢有益菌群移植技術 2025-07-12
- 海南光系統II葉綠素熒光儀 2025-07-12
- 天津婦科凝膠制造商 2025-07-12
- 分析試劑牌子 2025-07-12
- 河南前鼻拭子出口企業 2025-07-12
- 大腸桿菌可溶蛋白表達發展前景 2025-07-12
- 吉林Fab合成文庫項目合作 2025-07-12
- 寧波Blatchford假肢廠 2025-07-12
- 河南一次性血液過濾器環氧乙烷滅菌 2025-07-12