揚州倍篤高鹽核酸酶廠家電話
基因藥物常用的AAV載體有三種生產方法,分別是三質粒瞬轉體系、桿狀病毒表達載體體系和包裝細胞體系。其中,20多年前開發的三質粒瞬轉表達技術仍然占據腺相關病毒AAV生產的主流地位,其三質粒分別是Helper質粒(含E2a/b、E4和VARNA基因)、目標基因表達質粒及輔助質粒(含Cap和Rep基因)。雖然AAV病毒載體的血清型不同,但AAV的生產流程基本一致,主要有質粒共轉宿主細胞HEK293、293細胞生產病毒顆粒、從細胞培養上清或/及細胞裂解液中收獲病毒載體、純化/制劑/無菌過濾/灌裝等流程。黃山高鹽核酸酶價格哪家好呢,歡迎咨詢上海倍篤生物 。揚州倍篤高鹽核酸酶廠家電話
桿狀病毒表達載體體系Baculovirus/Sf9(Baculovirusexpression vector,BEV),是應用桿狀病毒表達載體(BEV)系統infect昆蟲細胞Sf9,是一種替代哺乳動物包裝細胞系的生產方案。整個系統包含兩種BEV,其中一個BEV攜帶兩側有ITRs的目的基因,另一BEV則攜帶rep/cap基因。這兩種BEV同時infectSf9即可組裝AAV。由于桿狀病毒具有輔助功能,因此BEV系統與可以穩定表達rep的Sf9細胞相結合,可用于靈活的、高滴度的大規模載體生產。BEV體系安全性好,infection效率高,生產工藝較之sTT更易放大,有更高的體積生產率優勢。商河倍篤高鹽核酸酶廠家徐州高鹽核酸酶售后服務哪家好呢,歡迎咨詢上海倍篤生物 。
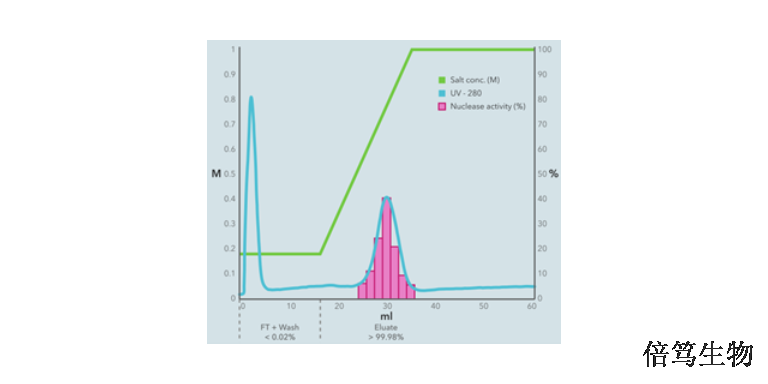
在不同的鹽濃度條件下,AAV病毒載體的存在形式不同。低鹽濃度條件下,AAV病毒顆粒表面會通過電荷作用等非特異結合到HCD上,從而產生病毒顆粒團聚現象。隨著溶液鹽濃度上升,AAV病毒顆粒與HCD的離子相互作用會被破壞,AAV病毒顆粒會逐漸解離。當鹽濃度升到更高范圍(>400mM左右),AAV病毒顆粒與HCD的結合更弱,AAV顆粒更穩定。因此,在高鹽濃度溶液中,AAV顆粒更加穩定,且有數據表明高鹽濃度不會削弱AAV的侵染能力。所以,我們推薦提高AAV病毒生產中的鹽濃度。
近年來,AAV在cancer疾病的醫治中顯示出巨大的價值。AAV作為基因藥物的載體已在肺、肝、眼、腦、肌肉等多個臨床試驗(超過100次)中得到應用,并在盲癥和血友病方面取得了巨大成功。2012年,AAV1載體編碼的脂蛋白脂肪酶成為歐盟批準的shou個用于醫治脂蛋白脂肪酶缺乏癥的基因產物(Glybera)。5年后,另一種AAV介導的基因藥物(Luxturna)隨后獲準在美國上市。基于AAV9的基因療(Zolgensma)也被用于醫治脊髓性肌肉萎縮。腺病毒在基礎和實驗研究有這么強的生命力原因在于:宿主范圍廣,對人致病率低;腺病毒粒子相對穩定,病毒基因重排頻率低;安全性高,不整合到染色體中,無插入致病基因,不干擾其他宿主基因。SAN HQ GMP是全球shou款市售GMP級別高鹽核酸酶,于2023年Q4上市。

目前基因藥物領域常用的病毒載體有腺病毒、慢病毒、重組腺相關病毒(rAAV)以及逆轉錄病du等,其中AAV因其免疫原性極低、安全性高、宿主細胞范圍廣、擴散能力強、表達穩定以及特異性強等優勢脫穎而出。據NIH統計,已有超過200個正在進行或已完成的基因藥物臨床試驗使用rAAV載體。盡管rAAV基因藥物已顯示出巨大的前景,但是強大、穩健而且可放大的基因載體生產制造工藝一直是CGT行業的痛點。目前rAAV生產平臺主要有三種:三質粒瞬轉體系(TransientTransfection, TT)、桿狀病毒表達載體體系(Baculovirusexpression vector,BEV)和包裝細胞體系(Packaging/Producercell line,PCL)。SAN HQ高鹽核酸酶具有熱不穩定的特性,在還原劑存在條件下,50℃、30min孵育即可失活;揚州倍篤高鹽核酸酶廠家電話
無錫高鹽核酸酶價格哪家好呢,歡迎咨詢上海倍篤生物 。揚州倍篤高鹽核酸酶廠家電話
在生物工藝中,核酸酶的主要作用是高效消化宿主細胞DNA(HCD),并將其分解成足夠小的片段,以便在下游純化過程中去除。雖然大多數核酸酶可以在生理鹽條件下高效地將裸DNA降解成微小片段,比如Benzonase和SANs都可以把dsDNA分解成小于8nt的寡核苷酸鏈,但實際生產中的核酸污染情況更加復雜。HCD通常以染色質形式存在,與細胞裂解碎片、病毒顆粒等結合在一起,影響核酸酶的識別及剪切。因此,HCD去除的關鍵在于——核酸酶如何在復雜的生產體系中識別并剪切HCD。 揚州倍篤高鹽核酸酶廠家電話
- 安徽70950-150中鹽核酸酶價格表 2025-07-23
- 廣東需求中鹽核酸酶廠家直銷 2025-07-23
- 無錫M-SAN HQ中鹽核酸酶工廠直銷 2025-07-23
- 安徽附近哪里有中鹽核酸酶 2025-07-23
- 天津哪些中鹽核酸酶聯系方式 2025-07-23
- 宿遷中鹽核酸酶代理商 2025-07-23
- 重慶綜合中鹽核酸酶廠家直銷 2025-07-23
- 南京70950-150中鹽核酸酶供應商 2025-07-23
- 安徽附近哪里有中鹽核酸酶銷售電話 2025-07-23
- 湖北ArcticZymes中鹽核酸酶 2025-07-23
- 湖州智能集中供水系統工作原理 2025-07-23
- 深圳牙科診所共享輪椅價格 2025-07-23
- 江蘇醫用醫療口腔拭子出口企業 2025-07-23
- 中山醫用內窺鏡模組 2025-07-23
- 國內藏香加盟 2025-07-23
- 青浦區染色價位 2025-07-23
- 上海婦產科虛擬仿真生產廠家 2025-07-23
- 揚州介紹人工智能輔助診斷設備24小時服務 2025-07-23
- 貴州蛋白質組學自動化設備源頭廠家 2025-07-23
- 溫州強腦智能假肢哪家便宜 2025-07-23