靠譜的eae模型有哪家
利用EAE動物模型,科學家們得以深入研究多發性硬化癥(MS)對大腦認知功能的影響及其潛在干預手段。這一模型能夠模擬MS患者大腦神經系統的病理變化,包括神經纖維的脫髓鞘、神經元損傷以及炎癥反應等,從而為我們提供了一個獨特的實驗平臺。通過觀察EAE動物模型在認知任務中的表現,科學家們能夠評估MS對大腦認知功能的損害程度,并探究其背后的神經生物學機制。同時,利用這一模型,科學家們還可以測試不同的干預手段,如藥物療愈、康復訓練等,以評估它們對改善認知功能的效果。因此,利用EAE動物模型深入研究MS對大腦認知功能的影響及其潛在干預手段,對于推動MS的臨床療愈和研究具有重要意義。NBP和BMSCs聯合可有效緩解EAE模型小鼠的癥狀。靠譜的eae模型有哪家
利用EAE動物模型,科學家們得以深入研究多發性硬化癥(MS)患者可能出現的神經系統功能障礙及其康復機制。這一模型通過模擬MS患者體內復雜的病理過程,為科學家們提供了一個獨特的實驗平臺。在EAE動物模型中,科學家們可以觀察到類似MS患者的神經系統受損情況,包括運動障礙、感覺異常以及認知功能下降等。通過對比模型動物與健康動物在行為學、神經生理學以及神經影像學等方面的差異,科學家們能夠揭示MS患者神經系統功能障礙的具體表現及其發生機制。同時,利用這一模型,科學家們還可以測試不同的康復療愈方法,評估其對于神經系統功能恢復的效果,為MS患者的康復療愈提供重要的實驗依據。因此,利用EAE動物模型研究MS患者可能出現的神經系統功能障礙及其康復機制,對于推動MS療愈的發展以及提高患者的生活質量具有重大意義。西藏大鼠eae模型造模方法EAE模型小鼠中致炎細胞Th17數量增加,抑炎細胞Treg和Breg數量降低。

實驗性自身免疫性腦脊髓炎(EAE)是一種以特異性致敏的CD4+T細胞介導為主的,以***系統內小血管周圍出現單個核細胞浸潤及髓鞘脫失為特征的自身免疫性疾病,是人類多發性硬化(MS)的理想動物模型,在臨床神經免疫學的研究中具有重要意義。抗原佐劑為非特異性免疫增強劑,它可改變抗原的物理性狀,延長抗原在體內的儲留時間,刺激抗原提呈細胞及淋巴細胞,從而增強和擴大免疫應答效果,它還能引起遲發性血腦屏障通透性增加和自身免疫反應。
MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突膠質細胞糖蛋白,髓鞘的一種微量成分,屬于免疫球蛋白超家族成員之一。t也是特定表達于***系統(CNS)的自身抗原,誘導多發性硬化癥的原發性脫鞘特征。MOG(35-55)是髓鞘少突膠質細胞糖蛋白的免疫優勢表位,能夠誘導強烈的T細胞和B細胞應激反應,具高度致腦炎性,能夠誘導嚙齒類動物的實驗性白身免疫性腦脊髓炎(EAE)模型。EAE是**普遍的MS動物模型,具有MS許多的臨床和病理生理學特征。單次注射MOG(35-55)能夠產生一種復發-緩解型神經性疾病,表現出大量斑塊狀脫髓鞘病癥。1-甲基-4-苯基-1,.2,3,6-四氫吡啶(MPTP)誘導的多巴胺神經元損傷模型,免疫接種MOG(35-55)能抑制該神經元的白發再生功能。MBP68-86可直接誘導Lewis大鼠形成EAE模型,無需任何佐劑[。
EAE動物模型的研究不僅為我們深入探索多發性硬化癥(MS)的發病機制提供了有力的工具,更在推動MS的臨床診斷和***技術方面發揮著舉足輕重的作用。通過對這一模型的深入研究,科學家們得以更***地了解MS的病理生理過程,從而為開發新的診斷方法提供了理論依據。同時,EAE動物模型也為評估新型***藥物的療效和安全性提供了重要的實驗平臺,為MS的臨床***提供了更為精細和個性化的方案。此外,隨著對EAE動物模型研究的不斷深入,我們有望在未來發現更多針對MS的有效***方法,為患者帶來更好的***效果和生活質量。因此,EAE動物模型的研究無疑將為MS的臨床診斷和***技術的進步注入新的動力。EAE通常用作細胞介導的特異性的自身免疫疾病的模型。西藏大鼠eae模型造模方法
EAE模型的被動轉移實驗是研究其發病機制的直接證據。靠譜的eae模型有哪家
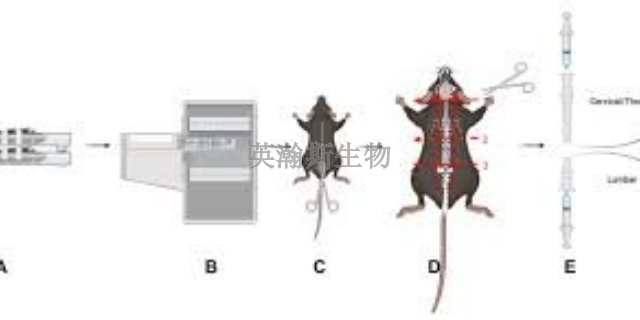
EAE模型是實驗動物通過神經組織(其中的某些成分)或病毒誘導產生的。EAE的誘導有主動誘導法和被動誘導法兩種。不同的免疫方法,可影響抗原遞呈,激發不同的免疫反應,這不但影響EAE的發生率,還可影響其發展與轉歸。通常采用主動誘導法制備EAE模型,將抗原與佐劑的混合乳劑直接注射至動物體內,經過一定時間的潛伏期,誘導EAE的產生。抗原注射部位的不同,可影響EAE的發生率、潛伏期、死亡率及復發率。常用的注射部位有腳墊、頸部及背部(皮下、皮內、肌肉)、腹腔和尾靜脈等多種,其中以皮下多點注射及腳墊注射的發病率比較高,而頸部注射則有較高的復發率。 因多次注射易引發免疫耐受,現在多采用單次注射抗原法。靠譜的eae模型有哪家
- 湖北eae模型實驗外包 2025-06-17
- 小鼠eae模型哪家口碑好 2025-06-17
- 浙江專門做eae模型如何構建 2025-06-17
- 浙江真實的eae模型有哪些 2025-06-17
- 西藏專門做eae模型實驗外包 2025-06-16
- 陜西比較好的eae模型有哪家 2025-06-16
- 甘肅比較好的eae模型 2025-06-16
- 四川真實的eae模型動物實驗外包 2025-06-16
- 河北eae模型怎么造模 2025-06-16
- 青海大鼠eae模型 2025-06-16
- 江西嬰兒鼻腔沖洗液產品 2025-06-17
- 廣東高純度海藻糖性狀 2025-06-17
- 石家莊市社康中心健康一體機生產廠家 2025-06-17
- 陜西特色洗鼻鹽加盟 2025-06-17
- 高分子活動義眼批發 2025-06-17
- 連江縣衛生室隨訪一體機廠家直銷 2025-06-17
- 清遠VR中醫針灸手法測試儀價格 2025-06-17
- 福建蛋白質組學自動化設備品牌 2025-06-17
- 河北同濟生物養胃益生菌 2025-06-17
- 醫用足壓多少錢 2025-06-17