江蘇比較好的eae模型造模方法
目前主要由三種髓鞘蛋白(或蛋白多肽)用于誘發EAE模型的研究:髓鞘少突膠質細胞糖蛋白(MOG),髓鞘堿性蛋白(MBP)和髓鞘蛋白脂質蛋白(PLP)※MBP是**早用來EAE研究的髓鞘抗原,多以誘發急性EAE(AcuteEAE)模型。※MOG是目前常用建立EAE模型的髓鞘抗原,多以誘發慢性EAE(ChronicEAE)模型※PLP也是常用建立EAE模型的髓鞘抗原,模型呈現緩解-復發的特點,多用來建立復發-緩解型(RelapseremittingEAERR-EAE)模型。以上三種是常見的誘導eae模型的蛋白。大多數小鼠EAE模型神經系統損害主要表現在脊髓。江蘇比較好的eae模型造模方法
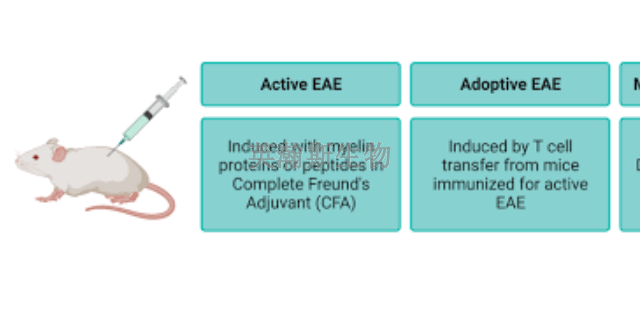
EAE動物模型的研究不僅對于多發性硬化癥(MS)的療愈具有重要的推動作用,更可能為其他神經系統疾病的研究提供寶貴的啟示。通過對EAE動物模型的深入研究,科學家們能夠更深入地理解神經系統疾病的發病機制,從而為開發新的療愈策略提供理論支持。同時,EAE動物模型在模擬神經系統疾病病理過程方面的成功應用,也為其他類似疾病的研究提供了可借鑒的經驗和方法。通過借鑒EAE動物模型的研究思路和技術手段,科學家們可以更加高效地開展其他神經系統疾病的研究,為這些疾病的診斷和療愈提供新的思路和方向。因此,EAE動物模型的研究不僅局限于MS的療愈,更有著廣泛的應用前景和深遠的意義。江西推薦的eae模型造模方法EAE模型是實驗動物通過神經組織(其中的某些成分)或病毒誘導產生的。
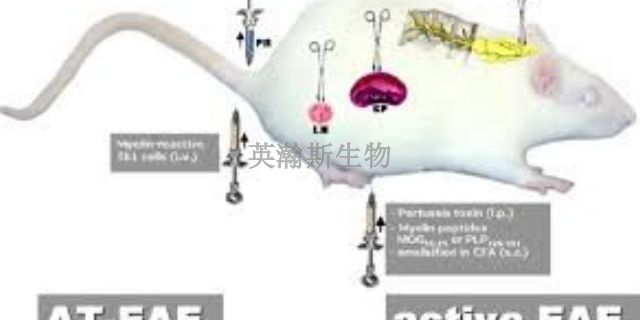
自身免疫性腦脊髓炎(EAE)模型是古老、比較常用的人類MS實驗模型。EAE包括了MS中觀察到的病理特征,包括:炎癥脫髓鞘軸突喪失神經膠質過多癥該模型還可以研究炎癥和髓鞘再生的解決反調節機制。但是,MS的每個方面都需要在EAE模型中進行單獨研究,增加了數據分析的難度。此外,研究中使用的不同試劑可能會導致不同程度的疾病。在小鼠中,使用不同濃度的百日咳***進行實驗性血液屏障損傷后,通過主動免疫誘導EAE。通過使用含有能夠***先天免疫系統的細菌成分的佐劑實現對髓磷脂抗原的敏感作用。由于人類中的活化抗原尚不清楚,因此使用多種CNS組織抗原如髓鞘堿性蛋白(MBP)、蛋白脂質蛋白(PLP139-151)或髓磷脂少突膠質細胞糖蛋白肽35-55(MOG35-55)誘導產生EAE。
從鳥類到哺乳類的多種動物如雞、小鼠、大鼠、豚鼠、家兔、羊、犬、猴等均可成功誘發EAE,但不同種屬或同一種屬不同品系動物的敏感性有很大差異。對EAE敏感的動物有Lewis、DA大鼠,PL/J、SJL/J小鼠,Hartley、Strain13豚鼠。雖然豚鼠對誘發EAE相當敏感,但其品系復雜,有關試劑缺乏,一般不常用作實驗對象。相比之下大鼠及小鼠的背景知識及相關試劑則較為普遍,遺傳學、免疫學等方面的研究也較深入,且其EAE在臨床、病理、免疫及生化改變等方面都與人類脫髓鞘疾病較為相似,因此應用比較為普遍。通常采用主動誘導法制備EAE模型,將抗原與佐劑的混合乳劑直接注射至動物體內。
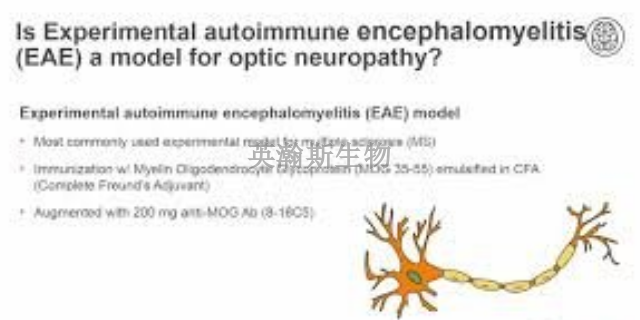
在EAE動物模型中,科學家們能夠觀察到一系列與多發性硬化癥(MS)極為相似的炎癥和神經損傷過程。這些過程不僅包括免疫細胞的浸潤和激發,還涉及神經纖維的脫髓鞘病變以及神經元的損傷和死亡。通過觀察EAE動物模型中的這些病理變化,科學家們能夠更加直觀地了解MS在人體內的發生機制,從而更加深入地探索疾病的本質。同時,這些觀察結果也為科學家們提供了研究MS的新思路和新方向,有助于推動MS的療愈和研究不斷取得新的進展。因此,EAE動物模型在揭示MS病理過程方面發揮著重要作用,為科學家們深入研究這一復雜疾病提供了有力的工具。EAE模型小鼠中致炎細胞Th17數量增加,抑炎細胞Treg和Breg數量降低。遼寧推薦的eae模型動物實驗外包
EAE模型是人類MS的經典動物模型,能夠為MS提供充分的實驗依據。江蘇比較好的eae模型造模方法
科學家們可以通過精心調控EAE動物模型的免疫反應,深入研究免疫療法在多發性硬化癥(MS)療愈中的潛在應用。在EAE動物模型中,科學家們能夠模擬MS患者體內免疫系統的異常反應,并通過一系列實驗手段,精細地調控免疫細胞的活性、數量和功能。通過觀察調控免疫反應后EAE動物模型的病情變化,科學家們能夠評估不同免疫療法對MS的療愈效果,并探索其背后的作用機制。這一研究不僅有助于揭示MS的發病機制,還為開發新的免疫療法提供了重要的實驗依據。因此,通過調控EAE動物模型的免疫反應來研究免疫療法在MS療愈中的應用,對于推動MS的療愈進展具有重要意義。江蘇比較好的eae模型造模方法
- 湖南大鼠eae模型如何構建 2025-06-26
- 內蒙古靠譜的eae模型是哪家 2025-06-26
- 福建eae模型怎么造模 2025-06-26
- 云南推薦的eae模型造模方法 2025-06-26
- 山西專業的eae模型如何構建 2025-06-26
- 江蘇比較好的eae模型造模方法 2025-06-26
- 四川專業的eae模型怎么造模 2025-06-26
- 重慶靠譜的eae模型有哪家 2025-06-26
- 上海大鼠eae模型哪家口碑好 2025-06-26
- 上海eae模型哪家口碑好 2025-06-26
- 奉賢區分子耗材牌子 2025-06-26
- 四川效果高鹽核酸酶銷售電話 2025-06-26
- 江門信息化按摩椅批發廠家 2025-06-26
- 寶山區現代健康管理咨詢 2025-06-26
- 人體器官芯片常見問題 2025-06-26
- 廣州解析柜環氧乙烷滅菌器產業鏈 2025-06-26
- 安徽益生元制造商 2025-06-26
- 北京70921-160高鹽核酸酶廠家直銷 2025-06-26
- 四川調理型益生菌作用 2025-06-26
- 南京試劑盒銷售廠家 2025-06-26