廣東小鼠eae模型如何構建
EAE模型是由針對CNS髓鞘發生免疫攻擊的CD4+Th1細胞介導的自身免疫性疾病,抗原致敏的T細胞穿過血腦屏障進入中樞,誘發對自身髓鞘抗原的免疫應答,導致腦及脊髓的免疫損傷。EAE是人類MS的經典動物模型,通過對EAE發病機制、病情發***展規律、臨床及病理改變、***及預防等方面的深入研究,能夠為MS的***提供充分的實驗依據。詞條圖冊EAE發病有多種誘發因素,包括食物、藥物及***等。大鼠的飼養環境級別越高,清潔度越高,接觸誘發因素的幾率越小,在相同條件下致敏,其發病率就越低,因此選用普通動物即可。**近有報道說明,EAE的發病還與動物的血腦屏障的形成有關。與對照組相比,EAE模型組小鼠脊髓中活化的小膠質細胞數量增多。廣東小鼠eae模型如何構建
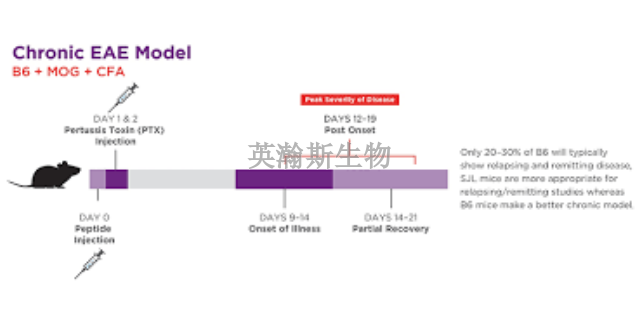
科學家們通過利用EAE動物模型,能夠深入探索多發性硬化癥(MS)發病過程中環境因素與基因因素之間的復雜相互作用。這一研究過程不僅有助于揭示MS的發病機理,還能為開發新的療愈策略提供重要線索。在EAE動物模型中,科學家們可以模擬不同的環境因素,如飲食、***等,觀察這些因素對模型動物神經系統的影響。同時,結合對模型動物基因表達的分析,科學家們可以進一步探究基因因素在MS發病中的作用,以及基因與環境因素之間的相互作用關系。通過對這些相互作用的深入研究,科學家們有望為MS的療愈和預防提供新的思路和方法。因此,利用EAE動物模型探索MS發病過程中的環境因素和基因因素的相互作用,對于推動MS研究的發展具有重要意義。廣東小鼠eae模型如何構建只有EAE的NHP模型才可以對人源性抗體進行臨床前評估。
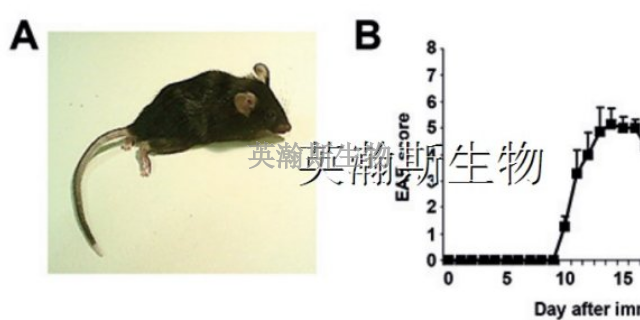
通過對EAE動物模型的基因表達分析,科學家們得以進一步深入了解多發性硬化癥(MS)的遺傳背景。這一分析過程涉及對模型動物體內基因表達水平的定量和定性研究,通過對比正常動物與EAE模型動物的基因表達差異,科學家們能夠識別出與MS發病相關的關鍵基因和基因網絡。這些基因可能涉及免疫調節、神經保護或修復等多個方面,它們的異常表達可能與MS的發病風險、疾病進程以及療愈效果密切相關。因此,對EAE動物模型進行基因表達分析不僅有助于揭示MS的遺傳機制,還為開發針對特定基因靶點的療愈方法提供了新的思路和方向。這一研究領域的進展將有助于我們更深入地認識MS這一復雜疾病,為未來的療愈和預防策略提供有力支持。
常用的致敏抗原有髓鞘堿性蛋白(MBP)或其多肽片斷(如MBP peptide 89—101)以及蛋白脂(PLP)等。長期以來MBP和PLP被認為是引起EAE和MS的主要抗原,MBP是髓鞘中抗原性比較強的蛋白質,占髓鞘總蛋白的40%,等電點在10以上,是強堿性蛋白質。研究表明MBP可***體內Th+細胞,使之穿過血腦屏障,攻擊自身神經髓鞘的MBP,從而導致***白質脫髓鞘,引起EAE模型或MS。近年來多用MBP肽代替MBP免疫動物。PLP是高度疏水的膜蛋白,對PLP不同肽決定簇發生反應的CD4+T細胞能誘導急性、慢性復發型及慢性進展型EAE。在MS患者體內也發現與PLP抗原決定簇發生反應的T細胞。 EAE模型的誘導方案比較繁雜,各種方案發病機制不盡相同。
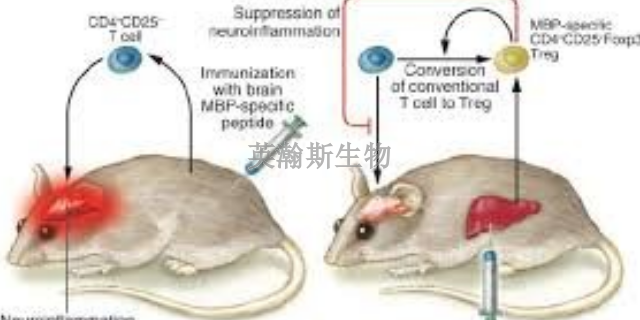
實驗性***反應性腦脊髓炎(EAE)是一種以特異性致敏的CD4+T細胞介導為主的,以***系統內小血管周圍出現單個核細胞浸潤及髓鞘脫失為特征的自身免疫性疾病,是人類多發性硬化(MS)的理想動物模型,在臨床神經免疫學的研究中具有重要意義。國內外學者試用多種易感動物建立EAE模型,以期闡明MS及EAE的發病機制,并為其病情的監測、復發的預防、治療方案的選擇以及新療法或新藥物的篩選等提供可靠依據。本文就近年來EAE模型方面的研究綜述如下。EAE能再現MS的很多臨床和病理特征。湖北推薦的eae模型動物實驗外包
將抗原與佐劑的混合乳劑直接注射至動物體內,經過一定時間的潛伏期,誘導EAE模型的產生。廣東小鼠eae模型如何構建
在EAE動物模型中,科學家們能夠觀察到一系列與多發性硬化癥(MS)極為相似的炎癥和神經損傷過程。這些過程不僅包括免疫細胞的浸潤和激發,還涉及神經纖維的脫髓鞘病變以及神經元的損傷和死亡。通過觀察EAE動物模型中的這些病理變化,科學家們能夠更加直觀地了解MS在人體內的發生機制,從而更加深入地探索疾病的本質。同時,這些觀察結果也為科學家們提供了研究MS的新思路和新方向,有助于推動MS的療愈和研究不斷取得新的進展。因此,EAE動物模型在揭示MS病理過程方面發揮著重要作用,為科學家們深入研究這一復雜疾病提供了有力的工具。廣東小鼠eae模型如何構建
- 西藏推薦的子宮內膜異位癥模型 2025-06-30
- 甘肅切片免疫組化外包 2025-06-30
- 湖北專門做eae模型是哪家 2025-06-30
- 寧夏靠譜的子宮內膜異位癥模型實驗外包 2025-06-29
- 內蒙古專門做eae模型有哪些 2025-06-29
- 四川靠譜的eae模型哪家口碑好 2025-06-29
- 廣東小鼠eae模型如何構建 2025-06-29
- 青海小鼠eae模型怎么造模 2025-06-29
- 重慶子宮內膜異位癥模型造模方法 2025-06-29
- 江蘇專門做子宮內膜異位癥模型哪家口碑好 2025-06-29
- 靜安區本地教育軟件設計 2025-06-30
- 甘肅分子耗材 2025-06-30
- 龍華區網絡共享輪椅聯系人 2025-06-30
- 湘潭超潤涂層應用 2025-06-30
- 安徽低溫環氧乙烷滅菌實驗 2025-06-30
- 中國澳門SP3蛋白組試劑盒 2025-06-30
- 安徽華晨陽細胞培養基廠家直銷 2025-06-30
- 無錫技術環氧乙烷滅菌方法 2025-06-30
- 山西民睿兒童義眼清洗 2025-06-30
- 上海墊底水門汀顏色 2025-06-30