香港克隆紡錘體卵質量評估
對于因疾病、年齡或其他原因可能失去生育能力的女性來說,MI期紡錘體卵冷凍技術提供了一種有效的生育能力保存方式。通過冷凍保存MI期卵母細胞并在適當的時候進行解凍和受精操作,可以實現生育愿望的延續。在輔助生殖技術中,MI期紡錘體卵冷凍技術可以用于提高試管嬰兒的成功率。通過選擇質量優良的MI期卵母細胞進行冷凍保存并在需要時進行解凍和受精操作,可以篩選出更具發育潛能的胚胎進行移植。MI期紡錘體卵冷凍技術還可以與遺傳病篩查技術相結合,通過檢測卵母細胞中的遺傳物質來篩選出健康的胚胎進行移植。這有助于降低遺傳病在后代中的發病率,提高出生人口的質量。紡錘體微管網絡的動態變化揭示了細胞分裂過程中分子層面的奧秘。香港克隆紡錘體卵質量評估
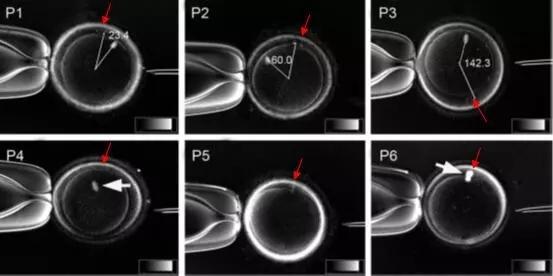
紡錘體的異常與多種疾病的發生和發展密切相關。例如,紡錘體形成或功能缺陷可能導致染色體分離錯誤,進而引發遺傳性疾病的發生。此外,紡錘體異常還可能影響細胞的增殖和分化能力,導致細胞增殖失控的發生。因此,深入研究紡錘體的形成機制和功能,對于揭示細胞分裂的調控機制、預防相關疾病具有重要意義。紡錘體作為有絲分裂過程中的精密“導航儀”,在細胞分裂中發揮著至關重要的作用。其結構、形成機制、功能以及精密導航作用的研究,不僅有助于揭示細胞分裂的復雜過程,還為預防相關疾病提供了新的思路和方法。未來,隨著細胞生物學和分子生物學技術的不斷發展,相信我們將對紡錘體的工作機制有更深入的認識和理解,為細胞分裂調控機制的研究和疾病提供更多的理論依據和實踐指導。香港無需染色紡錘體研究紡錘體有助于理解細胞分裂的分子機制。
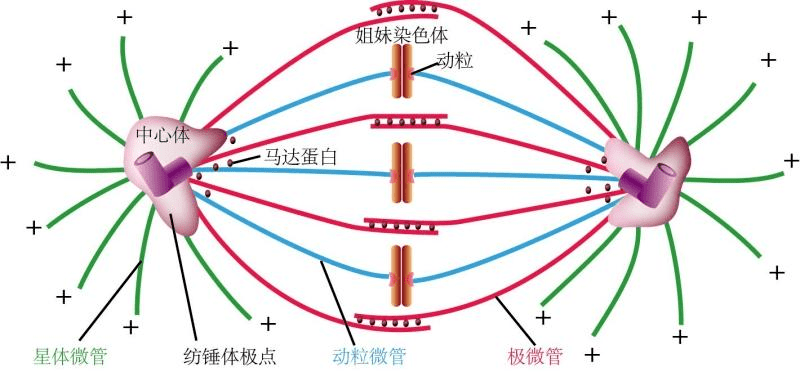
在有絲分裂過程中,紡錘體的形成和功能是高度協調的。從前期到中期,紡錘體逐漸成熟,染色體被精確排列在細胞的中間區域。到了后期和末期,紡錘體開始分解,將染色體拉向細胞的兩極,并完成胞質分裂。這一過程中,紡錘體的微管通過縮短和伸長來協調染色體的移動和定位,確保遺傳信息的準確傳遞。雖然無絲分裂過程中不形成明顯的紡錘體結構,但紡錘體的相關成分(如微管和動力蛋白)仍在細胞分裂中發揮作用。例如,在質體分裂中,紡錘體成分同樣起到了精確定位和運動染色體的作用。在減數分裂過程中,紡錘體的形成和功能更加復雜。以人卵母細胞為例,其紡錘體在減數分裂過程中會經歷一段較長時間的“多極紡錘體”階段,而后才形成雙極狀紡錘體。這一過程需要多種關鍵蛋白(如HAUS6、KIF11和KIF18A)的參與和調控。紡錘體的正確組裝和雙極化對于保證卵母細胞的正常發育和受精至關重要。
紡錘體在有絲分裂中發揮著至關重要的導航作用,其主要功能包括:排列與分裂染色體:紡錘體的完整性決定了染色體分裂的正確性。在細胞分裂中期,染色體在紡錘絲的牽引下,自動在赤道板排列整齊。當細胞進入分裂后期,紡錘體微管收縮,將染色體牽引至兩極,形成兩組數目相等的姐妹染色單體。這一過程確保了遺傳信息的準確傳遞,避免了染色體分離錯誤導致的遺傳異常。決定胞質分裂的分裂面:在染色體分裂的同時,紡錘體中的一部分微管不隨染色體分裂到兩極,而是停弛在紡錘體中間形成紡錘中心體。紡錘中心體的中心區域為兩組極性相反的微管交疊區,稱為紡錘中心區,它決定了接下來的胞質分裂面。胞質分裂開始于分裂后期的較晚期,一般結束于分裂末期后1-2小時,此期間兩個子細胞由中心顆粒體連接。紡錘體通過精確控制胞質分裂面的位置,確保了細胞分裂的對稱性和穩定性。紡錘體微管的動態變化是細胞分裂過程中引人注目的現象之一。
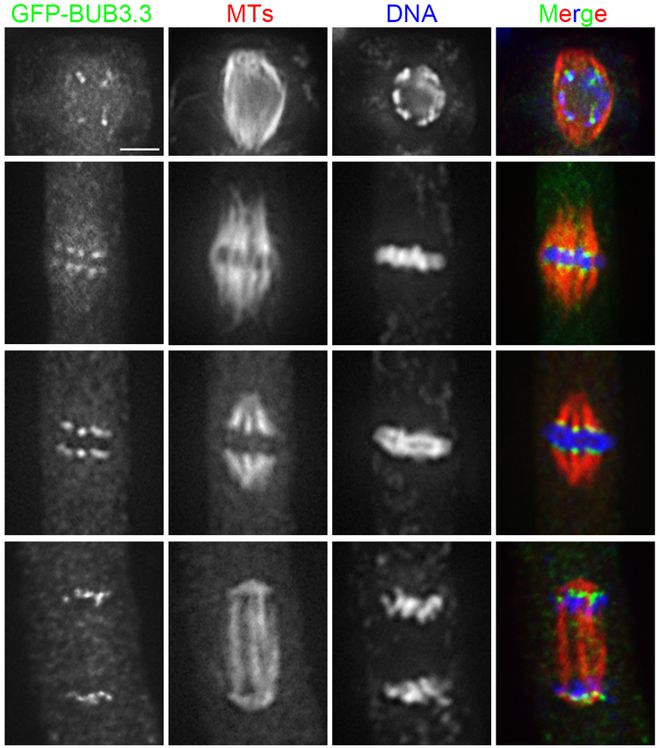
紡錘體的形成是一個復雜而精細的過程,涉及多種蛋白質的參與和調控。在有絲分裂的前間期,細胞進入S期,中心體開始復制倍增,為接下來的紡錘體形成做準備。進入G2期后,中心體完成復制,并在細胞進入分裂前期時分離,每個中心體各自形成放射狀排列的微管,即星體。這些微管通過持續增加和丟失組成微管的微管蛋白亞基,實現微管的聚合和解聚,使紡錘體得以形成和維持。微管的組裝和去組裝過程受到多種調節蛋白的精確調控,如蛋白激酶、磷酸酶等。這些調節蛋白能夠影響微管蛋白的聚合和解聚速率,從而控制紡錘體的形態和穩定性。此外,紡錘體的形成還依賴于動粒微管與染色體動粒的結合,這一過程由動粒上的驅動蛋白和動力蛋白介導,確保了染色體能夠被紡錘體正確地捕獲和牽引。顯微鏡下的紡錘體,如同精密的分子機器,引導染色體分離。香港無需染色紡錘體改善分級
紡錘體在減數分裂中也發揮重要作用,確保生殖細胞染色體正確分離。香港克隆紡錘體卵質量評估
基因編輯技術是一種可以精確修改基因序列的方法,如CRISPR/Cas9、TALENs和ZFNs等。這些技術已經被廣泛應用于基因領域,并取得了明顯的成果。在修復紡錘體異常方面,基因編輯技術可以通過精確修改導致紡錘體異常的致病基因,從而恢復紡錘體的正常功能。例如,針對某些遺傳性疾病中紡錘體相關基因的突變,基因編輯技術可以直接修復這些突變,從而來改善患者的病情。基因轉移是將正常基因導入到患者細胞中,以替代或補充致病基因的方法。香港克隆紡錘體卵質量評估
- 狗精子分析WOB 2025-07-05
- 北京計算機輔助精子分析BCF 2025-07-05
- 香港濃度精子分析VSL 2025-07-05
- 上海山羊精子分析BCF 2025-07-05
- 美國水生動物精子分析VAP 2025-07-05
- 北京牛精子分析LIN 2025-07-04
- 偏光成像紡錘體 2025-07-04
- 昆明雙折射性紡錘體提高冷凍保存效率 2025-07-04
- 武漢ICSI紡錘體Oosight Basic 2025-07-04
- 香港克隆紡錘體液晶偏光補償器 2025-07-04
- 狗精子分析WOB 2025-07-05
- 地質巖心光譜儀實驗室分析儀器 2025-07-05
- 天水VOC在線監測價格 2025-07-05
- 江西正規GXGS801多少錢 2025-07-05
- 檢測直線位移傳感器量大從優 2025-07-05
- 三節精鑄卡箍德標 2025-07-05
- 山東高壓設備維修哪家強 2025-07-05
- 南京DP2000燒錄器機器 2025-07-05
- 農業研究所培養箱價格 2025-07-05
- 江蘇哪些激勵器價格表 2025-07-05