南京正規外泌體提取試劑
外泌體鑒定:外泌體分離之后,需要經過一系列鑒定才能確定分離的是外泌體。鑒定方法從物理特征到表面分子標志物,多角度進行鑒定。l透射電鏡鑒定法:簡稱TEM,適合外泌體雙層囊膜超微結構觀察,即通常為茶托型或一側凹陷的半球形。l納米顆粒追蹤分析法:簡稱NTA,該方法能保證外泌體原始狀態、檢測速度快,檢測后能提供外泌體粒徑和濃度信息。lWesternblot分子標志物檢測:外泌體標志蛋白包括四跨膜蛋白家族,如CD9、CD63和CD81;細胞質蛋白,如肌動蛋白(Actin)和鈣磷脂結合蛋白(Annexins);使用可截留100KD分子量的膜,通過離心截留上清中的外泌體,截留完成后外泌體的提取方法學規范、統一定量及鑒定等。南京正規外泌體提取試劑

外泌體:已經有研究報道了各種Hh的胞外轉運機制,但實際用于體內Hh分泌和轉運的途徑尚不清楚。該研究顯示Hh在果蠅翅膀成蟲盤的分泌依賴于運輸所需的內體分選復合物(ESCRT)。在體內,產生Hh的細胞中ESCRT活性的降低導致外部細胞表面保留Hh。此外,產生Hh的細胞中的ESCRT活性對于長距離信號傳導是必需的。證據表明Hh和ESCRT蛋白質的庫在體內一起分泌到細胞外空間中,并且隨后可以在受體細胞的表面一起被檢測到。這些發現揭示了ESCRT蛋白質在控制形態發生活性中的新功能,揭示了一種新的機制,通過細胞外囊泡在組織中轉運分泌的Hh,這是長距離靶向誘導所必需的。北京正規外泌體提取試劑銷售廠家可以使用NanoSight?或電子顯微鏡分析純化的外泌體,以評估近似外泌體大小范圍和濃度。
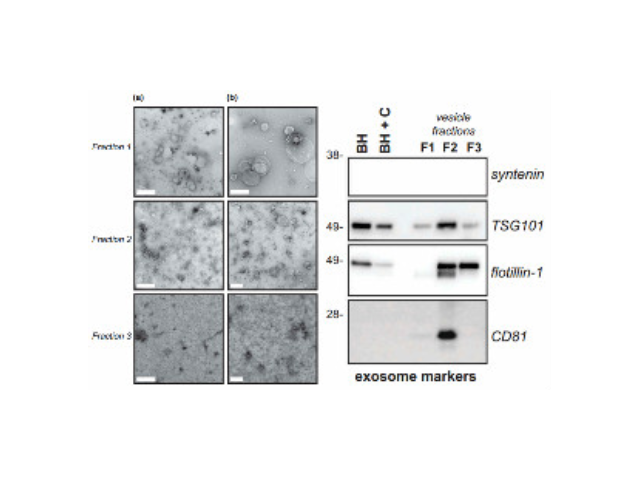
外泌體的提取、分離方法:尺寸排阻色譜法和超濾法;尺寸排阻色譜法是利用分子篩理論,較初是根據蛋白質分子大小分離蛋白質的色譜技術。該方法的主要優點是不需要很大的離心力,從而保證了外泌體的完整性。Mol等[13]對比超高速離心和尺寸排阻色譜法得到的外泌體蛋白,結果顯示,后者得到的外泌體的蛋白豐度高于前者。這些基于過濾或尺寸排阻色譜的新方法為外泌體大規模的生產和臨床應用提供了可能。超濾也是根據外泌體的尺寸將其分離出來的一種方法,超濾一般被認為是外泌體分離過程中的一個準備過程,通過超濾除去大分子和小分子的蛋白質。不過連續的超濾可以分離出外泌體,和超高速離心相比,超濾不需要特殊的設備就可以較短時間內分離出外泌體。但是,超濾膜對外泌體的黏附作用會降低外泌體的產量,并且超濾過程中施加的外力可能會使外泌體變形或者破裂。
專利申請利用分離培養人尿液來源細胞并收集培養基來進行體外培養,直接把外泌體從尿液中沉降下來,無須分離培養人尿液來源細胞并收集培養基。人尿液來源細胞的外泌體的獲取方法,是首先分離培養人尿液來源細胞并收集培養基,將人尿液來源細胞的培養基通過0.22微米濾膜過濾,以去除大的細胞殘片以及其它雜質;然后離心除去細胞器,留取上清;再使用可截留100KD分子量的膜,通過離心截留上清中的外泌體,截留完成后,使用PBS對膜進行洗脫即得到外泌體濃縮液。外泌體提取色譜法是利用根據凝膠孔隙的孔徑大小與樣品分子尺寸的相對關系而對溶質進行分離的分析的方法。
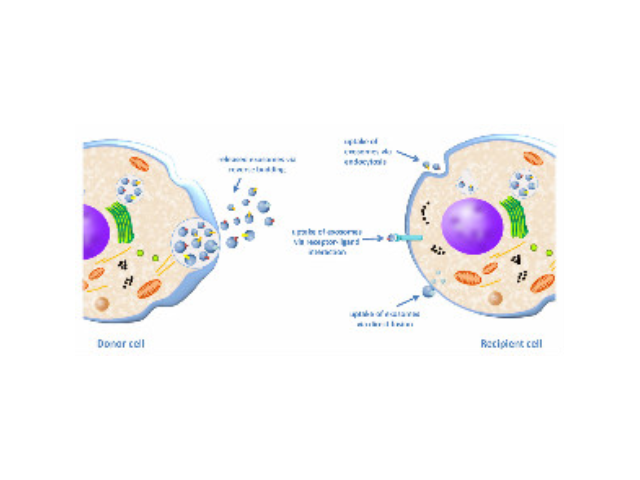
研究初次發現瘧原蟲傳染小鼠血漿外泌體(exosomes)能夠壓制一些病癥血管生成,并初步闡明其分子機制。研究加深了對瘧原蟲傳染宿主所分泌的外泌體與一些病癥血管生成之間的相互作用的認識,為開發瘧原蟲傳染來源的外泌體作為一種新型抗一些病癥制劑奠定了基礎。研究人員選用肺病小鼠模型作為研究對象,從傳染瘧原蟲的小鼠血漿中獲得外泌體,并將這些外泌體注射到小鼠的一些病癥內部,并與沒有瘧原蟲傳染的小鼠血漿外泌體進行對照。研究發現,瘧原蟲傳染小鼠的血漿外泌體明顯壓制一些病癥血管的生成。進一步的研究發現,瘧原蟲傳染的小鼠血漿外泌體通過至少四種特殊的微小RNA(miR16-5p/17-5p/322-5p/497-5p)壓制血管內皮細胞VEGF受體(VEGFR2)的表達從而阻斷血管生成的信號通路。這些發現加深了人們對瘧原蟲抗病機理的理解,并為瘧原蟲療法治病一些疾病的臨床研究提供進一步的理論依據。外泌體的提取方法:密度梯度離心。廈門正規外泌體提取試劑推薦廠家
外泌體提純試劑盒的特色與優勢:無需耗時的超速離心,過濾或特殊注射器。南京正規外泌體提取試劑
外泌體的生物學功能研究中需要分離完整的外泌體顆粒,而傳統超速離心方法步驟繁瑣、硬件要求高、操作難度大。李記生物自主開發的外泌體快速提取試劑盒,組分經過優化處理,適用于細胞培養上清液、血清、血漿、尿液及其他體液(腦脊液、腹水、羊水、乳汁以及唾液等)中的外泌體提取,并搭配純化過濾裝置,可快速高效地獲得高純度外泌體顆粒。注意事項:1.對于待測樣品粘度過大時,可將樣本用4℃預冷的1×PBS緩沖液進行等體積稀釋處理。2.當血清、血漿、唾液等樣品收獲的外泌體濃度較高,收獲的外泌體顆粒無法通過EPF柱純化時,可用4℃預冷的1×PBS進行稀釋后再通過EPF柱離心。南京正規外泌體提取試劑
- 杭州正規外泌體提取試劑平均價格 2025-07-30
- 廈門正規外泌體提取試劑推薦廠家 2025-07-30
- 鄭州正規外泌體提取試劑服務電話 2025-07-30
- 鄭州無血清細胞凍存液哪里買 2025-07-30
- 金華正規外泌體提取試劑 2025-07-30
- 南京正規外泌體提取試劑 2025-07-30
- 徐州正規無血清細胞凍存液哪家便宜 2025-07-30
- 無錫外泌體提取試劑生產廠家 2025-07-30
- 上海正規外泌體提取試劑平均價格 2025-07-30
- 南京正規無血清細胞凍存液哪家好 2025-07-30
- 淮安電感用環氧粉末膠銷售電話 2025-07-30
- 黑龍江柔順劑代加工 2025-07-30
- 杭州硅橡膠密封膠條品牌 2025-07-30
- 湖州底盤運動平臺銷售品牌 2025-07-30
- 廣州植物基1.3-丁二醇銷售公司 2025-07-30
- 合肥無磷水性清洗劑代加工 2025-07-30
- 附近甲苯市價 2025-07-30
- 武漢細胞培養核孔膜供應商 2025-07-30
- 襄陽CT型(硅)耐熱涂料商家 2025-07-30
- 銅陵工業級消光粉生產工藝 2025-07-30